- Зохиолч Alex Aldridge aldridge@what-difference.com.
- Public 2023-12-17 13:45.
- Хамгийн сүүлд өөрчлөгдсөн 2025-06-01 07:37.
Гидразин ба карбогидразидын гол ялгаа нь гидразин нь H2N-NH2 бүтцийг агуулдаг бол карбогидразид нь нэг карбонилийн нүүрстөрөгчийн төвд холбогдсон хоёр гидразин молекулыг агуулдаг.
Гидразин ба карбогидразид нь H2N-NH2 нэгж агуулсан химийн нэгдлүүд юм. Энэхүү химийн бүтцийн нэг нэгжийг гидразин гэж нэрлэдэг бол карбогидразид нь карбонил нүүрстөрөгчийн төвд эдгээр хоёр бүтэцтэй байдаг.
Гидразин гэж юу вэ?
Гидразин нь N2H4 химийн томъёотой органик бус нэгдэл юм. Бид үүнийг энгийн пниктоген гидрид гэж нэрлэж болох бөгөөд энэ нь аммонийн үнэртэй, өнгөгүй, шатамхай шингэн юм. Энэ нэгдэл нь маш хортой тул бид энэ бодистой болгоомжтой харьцах ёстой. Хэрэв уусмалд хэрэглэвэл түүний хоруу чанар буурна, жишээлбэл. гидразин гидрат.

Зураг 01: Гидразин гидрат
Гидразин нь полимер хөөс бэлтгэхэд чухал ач холбогдолтой хөөс үүсгэгчийн хувьд голчлон хэрэгтэй. Түүнчлэн, энэ нь полимержих катализатор, эм, агрохимийн урьдал бодис болохоос гадна сансрын хөлгийг хөдөлгөхөд удаан хугацаагаар хадгалах боломжтой түлш юм.
Гидразин үйлдвэрлэх олон янзын арга байдаг, үүнд хэт исэлээс аммиакийг оксазиридинаар исэлдүүлэх, хлор дээр суурилсан исэлдүүлэх гэх мэт. Гидразин үүсэх урвалыг авч үзэхэд гидразин нь хүчил-суурь үүсгэдэг болохыг харуулж байна. моногидрат нь усгүй хэлбэрээс илүү нягт бөгөөд аммиактай харьцуулахуйц үндсэн (шүлт) шинж чанартай байдаг. Нэмж дурдахад гидразин нь редукторын үүрэг гүйцэтгэж, ихэвчлэн азот, ус зэрэг дайвар бүтээгдэхүүн үүсгэдэг тул исэлдэлтийн урвалд орж болно.
Нүүрстөрөгчид гэж юу вэ?
Нүүрс ус нь H4N2-C(=O)-N2H4 химийн томъёотой органик нэгдэл юм. Энэ бодис нь цагаан, усанд уусдаг хатуу бодис шиг харагддаг бөгөөд хайлах үед задралд ордог. Нэг буюу хэд хэдэн N-H бүлгийг өөр орлуулагчаар сольсон хэд хэдэн карбазид байдаг.
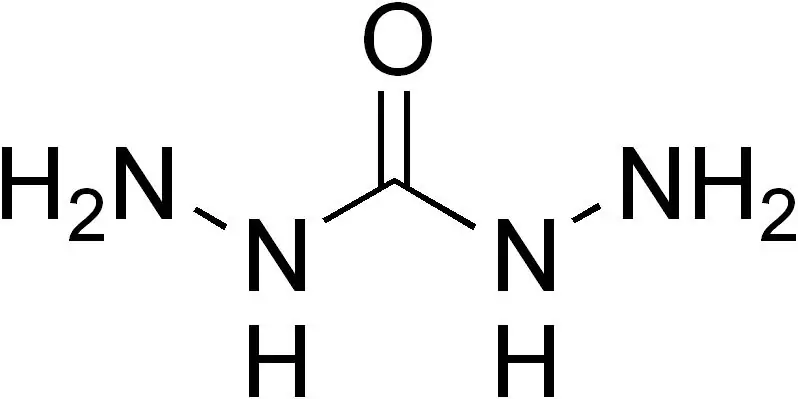
Зураг 02: Нүүрс устөрөгчийн молекулын бүтэц
Бид энэ бодисыг мочевиныг гидразинээр боловсруулснаар үйлдвэрийн аргаар гаргаж авах боломжтой. Мөн бид энэ бодисыг бусад C1 прекурсоруудыг гидразин, түүний дотор карбонатын эфиртэй урвалд оруулан бэлтгэж болно.
Нүүрс устөрөгчийн молекул нь туйлт бус молекул бөгөөд энэ молекул дахь бүх азотын төвүүд нь бага зэрэг пирамид хэлбэртэй байдаг нь C-N pi холболт сул байгааг харуулж байна.
Энэ нэгдлийн хэрэглээг авч үзэхэд хүчилтөрөгч цэвэрлэгч, полимерийн урьдал бодис, гэрэл зурагт тогтворжуулагч, сумны түлш үйлдвэрлэх, саван тогтворжуулах гэх мэт чухал ач холбогдолтой.
Гидразин ба карбогидразидын хооронд ямар ялгаа байдаг вэ?
Гидразин ба карбогидразид нь азот агуулсан химийн нэгдлүүд юм. Гидразин ба карбогидразидын гол ялгаа нь гидразин нь H2N-NH2 бүтцийг агуулдаг бол карбогидразид нь нэг карбонил нүүрстөрөгчийн төвд холбогдсон хоёр гидразин молекулыг агуулдаг. Цаашилбал, бид гидразиныг органик бус нэгдэл, нүүрсбогидразидыг органик нэгдэл гэж ангилж болно, учир нь гидразин нь молекулуудад нүүрстөрөгчийн атомгүй байдаг ч карбогидразид нь нүүрстөрөгчийн төвийг агуулдаг.
Түүнээс гадна бид хэт исэл, хлор дээр суурилсан исэлдэлт гэх мэтээр аммиакийг исэлдүүлэх замаар аммиакийг исэлдүүлэх замаар гидразин, мочевиныг гидразинээр эмчлэх замаар нүүрсбогидразидыг гаргаж авах боломжтой.
Доорх инфографик нь гидразин ба карбогидразидын ялгааг хүснэгт хэлбэрээр харуулж байна.

Хураангуй - Гидразин ба Карбогидразид
Гидразин ба карбогидразид нь азот агуулсан химийн нэгдлүүд юм. Гидразин ба карбогидразидын гол ялгаа нь гидразин нь H2N-NH2 бүтцийг агуулдаг бол карбогидразид нь нэг карбонил нүүрстөрөгчийн төвд холбогдсон хоёр гидразин молекулыг агуулдаг. Түүнчлэн гидразин нь өнгөгүй шингэн хэлбэрээр, харин карбогидразид нь цагаан өнгөтэй хатуу бодис хэлбэрээр үүсдэг.






