- Зохиолч Alex Aldridge aldridge@what-difference.com.
- Public 2023-12-17 13:45.
- Хамгийн сүүлд өөрчлөгдсөн 2025-06-01 07:37.
Нүүрстөрөгчийн хүчил ба бикарбонатын гол ялгаа нь нүүрстөрөгчийн хүчил нь төвийг сахисан химийн нэгдэл, харин бикарбонат нь сөрөг цэнэгтэй химийн нэгдэл юм.
Нүүрстөрөгчийн хүчил нь нүүрстөрөгчийн давхар ислийг усанд уусгахад уусмалд үүсдэг сул хүчил бөгөөд H2CO3 химийн томьёотой. Бикарбонат нь хүчилтөрөгчийн гурван атом, устөрөгчийн атом, нүүрстөрөгчийн атомын нэгдэлд HCO3- химийн томьёотой үүснэ.
Нүүрстөрөгчийн хүчил гэж юу вэ?
Нүүрстөрөгчийн хүчил нь H2CO3. Заримдаа бид ус эсвэл карбонатлаг усанд ууссан нүүрстөрөгчийн давхар исэл агуулсан уусмалд энэ нэрийг өгдөг. Учир нь хийжүүлсэн усанд бага хэмжээний H2CO3 агуулагддаг. Цаашилбал, нүүрстөрөгчийн хүчил нь сул хүчил бөгөөд энэ нь карбонат ба бикарбонат гэсэн хоёр төрлийн давс үүсгэдэг. Энэ нэгдлийн молийн масс нь 62.024 г/моль.
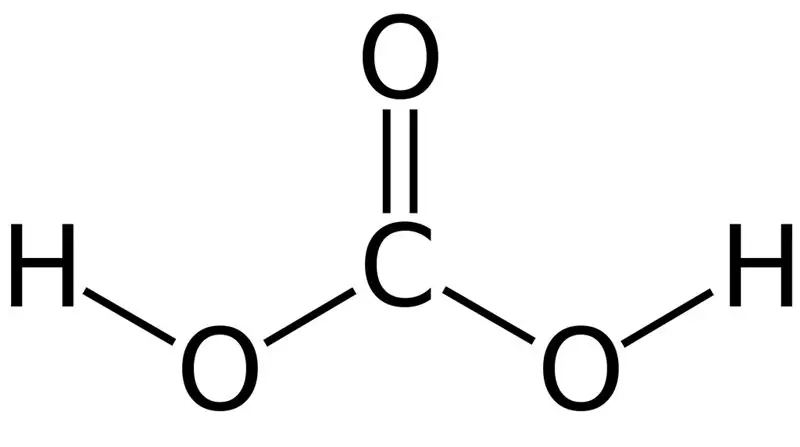
Зураг 01: Нүүрстөрөгчийн хүчлийн химийн бүтэц
Нүүрстөрөгчийн давхар исэл усанд уусах үед нүүрстөрөгчийн давхар исэл ба нүүрстөрөгчийн хүчлийн тэнцвэрт байдалд ордог. Тэнцвэр нь дараах байдалтай байна:
CO2 + H2O ⟷ H2CO3
Хэрэв бид суурь дээр илүү их нүүрстөрөгчийн хүчлийг нэмбэл бикарбонат болно. Гэхдээ хэрэв суурь нь илүүдэл байвал нүүрстөрөгчийн хүчил нь карбонатлаг давс өгөх хандлагатай байдаг. Илүү нарийвчлалтайгаар нүүрстөрөгчийн хүчил нь карбонил нүүрстөрөгчтэй хавсарсан хоёр гидроксил бүлгийн орлуулагчтай карбоксилын хүчлийн нэгдэл юм. Түүнээс гадна энэ нь протоныг өгөх чадвартай полипротик хүчил юм. Энэ нь зөөврийн хоёр протонтой тул тусгайлан дипротик юм.
Бикарбонат гэж юу вэ?
Бикарбонат нь хүчилтөрөгчийн гурван атом, устөрөгч, нүүрстөрөгчийн атомуудын нэгдлээс үүсдэг. Энэ хослолын бүтээгдэхүүн нь ион эсвэл протоноос илүү электронтой нэгдэл байж болно. Бид үүнийг HCO3- химийн томьёотой химийн төрөл зүйл гэж тодорхойлж болно.
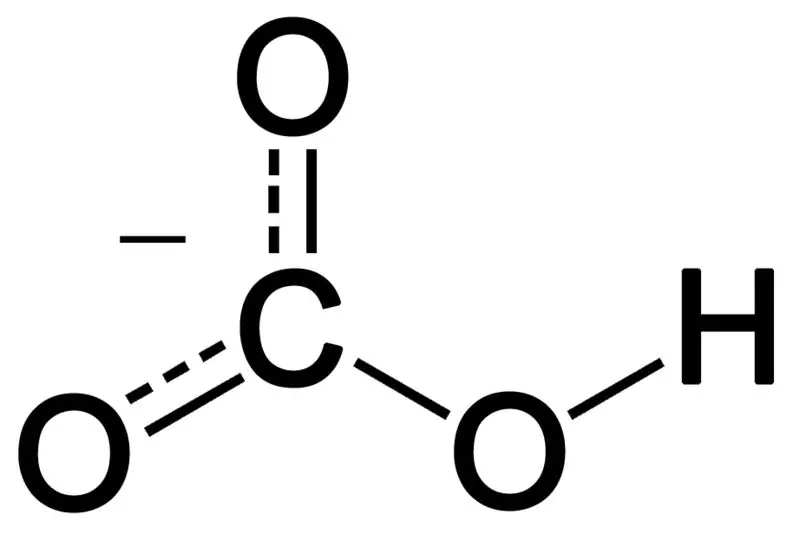
Зураг 02: Бикарбонатын анионы химийн бүтэц
Энэ нэгдэл нь хүний биеийн рН-ийн буферийн системийн чухал хэсэг бөгөөд энгийн үгээр хэлбэл: цусыг хэт хүчиллэг эсвэл хэт суурь биш байдалд байлгах үүрэгтэй. Нэмж дурдахад энэ нь ходоод нь хоолоо шингээж дууссаны дараа хоол боловсруулах шүүсийг хянах арга болдог. Цаашилбал, борооны усанд агуулагдах нүүрстөрөгчийн хүчил чулуулагт цохиулах үед бикарбонатын ион үүсгэдэг. Бикарбонатын ионуудын энэ урсгал нь нүүрстөрөгчийн эргэлтийг үргэлжлүүлэхэд чухал юм.
Нүүрстөрөгчийн хүчил ба бикарбонат хоёрын ялгаа юу вэ?
Нүүрстөрөгчийн хүчил нь нүүрстөрөгчийн давхар ислийг усанд уусгахад уусмалд үүсдэг сул хүчил бөгөөд химийн томъёо нь H2CO3 юм. Бикарбонат нь хүчилтөрөгчийн гурван атом, устөрөгчийн атом ба нүүрстөрөгчийн атомыг нэгтгэснээр HCO3- химийн томъёогоор үүсдэг. Нүүрстөрөгчийн хүчил ба бикарбонатын гол ялгаа нь нүүрстөрөгчийн хүчил нь төвийг сахисан химийн нэгдэл, харин бикарбонат нь сөрөг цэнэгтэй химийн нэгдэл юм. Мөн нүүрстөрөгчийн хүчлийг хөөстэй, хийжүүлсэн ундаа хийх, арьсны дерматит эмчлэх, ам зайлах гэх мэт, харин бикарбонатыг жигнэх зэрэг хүнсний бүтээгдэхүүнд (исгэх бодис болгон) ашигладаг бөгөөд рН-ийн өөрчлөлтийг эсэргүүцэх чадварыг өгдөг.
Дараах инфографик нь нүүрстөрөгчийн хүчил ба бикарбонат хоёрын ялгааг зэрэгцүүлэн харьцуулахын тулд хүснэгт хэлбэрээр нэгтгэн харуулав.
Тойм - Нүүрстөрөгчийн хүчил ба бикарбонат
Нүүрстөрөгчийн хүчил нь H2CO3. Бикарбонат нь гурван хүчилтөрөгчийн атом, устөрөгчийн атом ба нүүрстөрөгчийн атомыг нэгтгэснээр HCO3- химийн томъёогоор үүсдэг. Нүүрстөрөгчийн хүчил ба бикарбонатын гол ялгаа нь нүүрстөрөгчийн хүчил нь төвийг сахисан химийн нэгдэл, харин бикарбонат нь сөрөг цэнэгтэй химийн нэгдэл юм.






