- Зохиолч Alex Aldridge aldridge@what-difference.com.
- Public 2023-12-17 13:45.
- Хамгийн сүүлд өөрчлөгдсөн 2025-06-01 07:37.
Нягт ба хувийн жингийн гол ялгаа нь нягт нь үнэмлэхүй утга, харин хувийн жин нь бодисын хувьд харьцангуй утга юм.
Нягт ба хувийн жин гэдэг нь ихэвчлэн хоорондоо андуурагддаг түгээмэл хэрэглэгддэг хоёр нэр томъёо юм. Ялангуяа үйлдвэрлэлийн салбарт эдгээр нэр томъёо нь янз бүрийн бодисыг жинлэх, шингэний концентрацийг тооцоолоход маш чухал юм. Энэ хоёрыг тооцоолоход температур, даралт маш чухал.
Нягт гэж юу вэ?
Материалын нягт гэж бидний түгээмэл нэрлэдэг массын нягт нь түүний нэгж эзэлхүүн дэх масс юм. Бид нягтралыг илэрхийлэхийн тулд P тэмдгийг ашигладаг бөгөөд SI нэгж нь нэг куб метр тутамд килограмм байна. Температур ба даралт нь нягтралд нөлөөлдөг хоёр хүчин зүйл юм; Жишээлбэл, бид даралтыг нэмэгдүүлэхэд объектын эзэлхүүн буурч, энэ нь тухайн объектын нягтыг нэмэгдүүлдэг. Үүний нэгэн адил, хэрэв бид объектын температурыг нэмэгдүүлэх юм бол эзлэхүүн нэмэгдэхийн хэрээр нягт нь буурдаг. Усны нягт нь 1.0 г / мл байна. Хэрэв объектын нягт нь усны нягтаас бага байвал тэр нь усны гадаргуу дээр хөвөх ба эсрэгээр.

Зураг 01: Обьект хөвөх эсвэл живэх эсэх нь түүний өөрийн нягт болон түүний байрлуулсан шингэний нягтаас хамаарна.
Хэрэв та бодисын хэмжээг нэмэгдүүлбэл массыг ихэсгэх боловч нягтралд нөлөөлөхгүй. Энэ нь бодисын нягт нь өвөрмөц бөгөөд үнэмлэхүй гэсэн үг.
Хувийн таталц гэж юу вэ?
Хувийн жин нь харьцангуй утга учир нэгжгүй. Энэ нь үнэндээ харьцангуй нягтралын өөр нэр томъёо юм. Энэ нь бодисын нягтыг жишиг бодисын нягттай харьцуулсан харьцаа бөгөөд энэ нь хатуу ба шингэний хувьд үргэлж ус, хийн хувьд энэ нь тэнцүү хэмжээний агаар эсвэл устөрөгч юм. Бид хувийн жинг SG гэж тэмдэглэж болно.
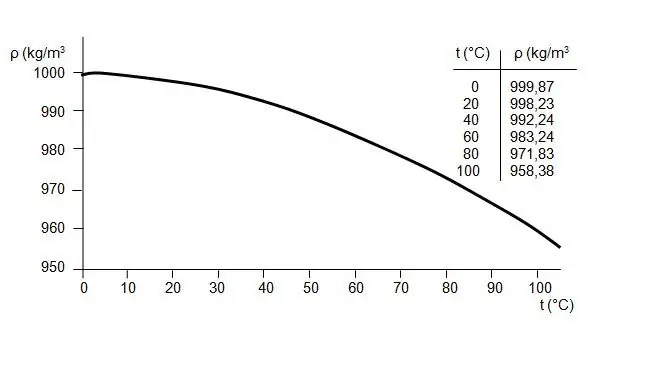
Зураг 02: Янз бүрийн температурт усны SG (энд SG-ийг “ρ” өгсөн)
Температур ба даралт нь 1 атм ба 4°С хэмийн стандарт даралттай хэмжигдэхүүн тул SG-ийг хэмжихэд чухал ач холбогдолтой. Аж үйлдвэр бүр өөрийн гэсэн стандарт, хэрэгцээтэй байдаг тул температур нь өөр өөр байж болно. Тусгай жин нь тодорхой зорилгоор үйлдвэрлэсэн уусмалын концентрацийг тооцоолоход ашигтай байдаг. Цаашилбал, бид стандарт температур, даралт дахь усны хувийн жинг 1 гэж үздэг тул хэрэв бодисын SG 5 бол энэ нь уснаас тав дахин нягт байна гэсэн үг юм. Тэр бодис нь усны ёроолд живнэ. Үүний нэгэн адил, хэрэв бодисын SG нэгээс бага бол усны гадаргуу дээр хөвөх болно.
Нягт ба хувийн таталцлын хооронд ямар төстэй зүйл байдаг вэ?
- Нягт ба хувийн жинг хэмжихдээ бид материалын массыг ашигладаг; тиймээс эдгээр нэр томъёо нь температур, даралтаас хамаардаг тул масс нь температур, даралтаас хамаардаг.
- Бид усны нягт ба SG-ийг 1 гэж авдаг.
- Зарим тохиолдолд бид нягтын утгыг SG утгаар илэрхийлдэг.
Нягт ба хувийн жингийн ялгаа нь юу вэ?
Нягт нь нэгж эзэлхүүн дэх материал юм. Хувийн жин гэдэг нь тухайн бодисын нягтыг жишиг бодисын нягттай харьцуулсан харьцаа юм. Нягт ба хувийн таталцлын гол ялгаа нь нягт нь үнэмлэхүй утга, харин хувийн жин нь бодисын хувьд харьцангуй утга юм. Бид ихэвчлэн нягтралыг "p", хувийн жинг "SG" гэж тэмдэглэдэг. Цаашилбал, нягтын хэмжүүр нь нэг шоо метр дэх килограмм бөгөөд SG нь харьцаа учраас нэгжгүй.
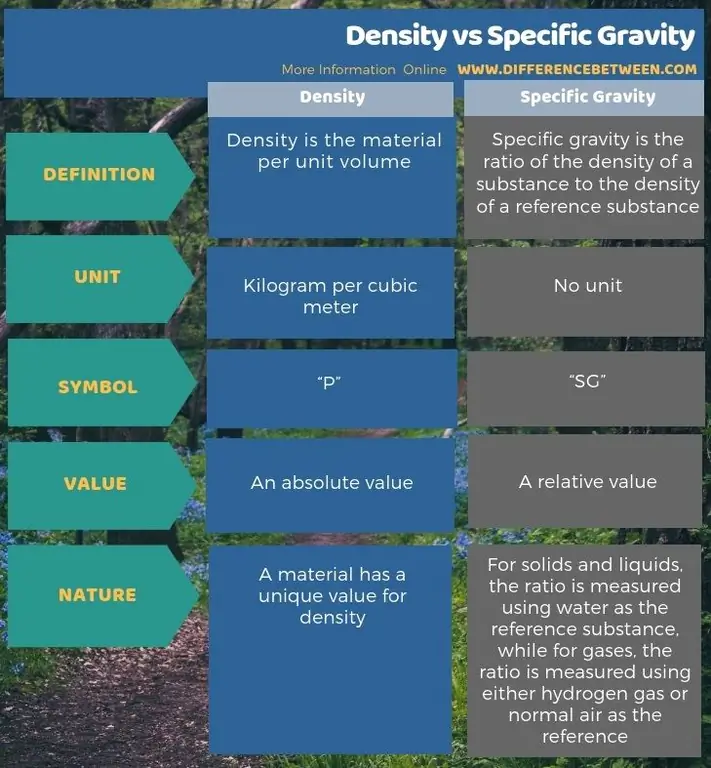
Тойм - Нягт ба хувийн жин
Нягт нь нэгж эзэлхүүн дэх материал бөгөөд хувийн жин нь тухайн бодисын нягтыг жишиг бодисын нягттай харьцуулсан харьцаа юм. Нягт ба хувийн жингийн гол ялгаа нь нягт нь үнэмлэхүй утга, харин хувийн жин нь бодисын харьцангуй утга юм.






